Fiebre Q
Diagnóstico
La inespecificidad de las manifestaciones clínicas hacen que el laboratorio tenga un rol fundamental en la detección de fiebre Q. Previo a ello, es importante obtener una historia detallada sobre la ocupación, contacto con animales o ingestión de alimentos de riesgo.
SEROLOGÍA
Ante la presentación de un caso sospechoso de fiebre Q, el estudio serológico por inmunofluorescencia es la técnica diagnóstica de elección, debido a que la respuesta inmune induce la producción de anticuerpos para las fases antigénicas I y II.
A pesar de existir grandes variaciones en esta respuesta inmune, la seroconversión ocurre generalmente después de la primera semana de iniciados los síntomas. Los anticuerpos de fase II son los primeros en desarrollarse, aumentando de manera casi simultánea los acnticuerpos IgM e IgG de esta fase. La mejor forma de estudiar un caso sospechoso de fiebre Q aguda es a través de la detección de anticuerpos de fase II 7 a 21 días después del inicio de los síntomas clínicos y luego evaluar su disminución después de 3 a 6 meses. Es confirmatorio de infección aguda el hallazgo de un aumento de 4 veces de los títulos de anticuerpos IgG o IgM de fase II, entre dos muestras de suero pareadas tomadas con una separación de 3 a 6 semanas. Debido a la gran variabilidad en la elevación de los anticuerpos es recomendable el estudio de al menos dos muestras de suero (una de la fase aguda y una de la fase convaleciente).
Los límites para un título serológico positivo pueden variar entre países. En general, un título de IgG de fase II de ≥1:64 es considerado sugerente para el diagnóstico de fiebre Q aguda. Los títulos de IgG de fase II tienden a ser más altos que los títulos de IgG de fase I durante la infección primaria. Independientemente de la sintomatología, los títulos de anticuerpos IgG residuales pueden ser detectables durante años e incluso de por vida. Se ha demostrado que el tratamiento precoz no influye en la posterior respuesta de IgG II.
De no contar con el estudio de muestras pareadas, una muestra positiva (IgG Fase II > 1:128) tomada en fase de convalecencia en un paciente con síntomas compatibles >1 semana de duración, es sugerente de infección aguda probable.
El Instituto de Salud Pública dispone de la prueba IFA para IgM/IgG fase II e IGM/IgG Fase I.
PCR
La prueba de reacción en cadena de la polimerasa (PCR) en sangre o suero, tiene baja sensibilidad, podría ser útil en las primeras 2 semanas después de la aparición de los síntomas y antes de la administración de antibióticos y en las formas crónicas de la enfermedad. Si bien un ensayo de PCR positivo podría confirmar el diagnóstico, un resultado de prueba de PCR negativo no descarta la fiebre Q.
Fiebre Q (infección por Coxiella burnetii). En Red Book Informe 2015 del comité sobre enfermedades infecciosas; Eldin, C et al. From Q fever to Coxiella burnetii Infection: a paradigm Change. Clinical Microbiology reviews. Vol 30(1): 115-171;
La detección de C. burnetii en tejidos mediante PCR también puede confirmar un diagnóstico de fiebre Q.
El Instituto de Salud Pública (ISP) cuenta con la detección de Coxiella por PCR en tiempo real en sangre y tejidos.
CULTIVO
Este microorganismo no crece en medios de cultivos habituales, los cuales suelen resultar negativos (hemocultivos u otros cultivos corrientes).
DETECCIÓN COXIELLA BURNETII EN CASOS SOSPECHOSOS
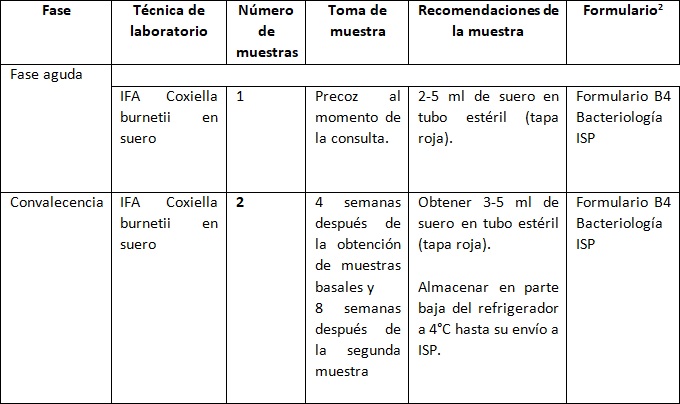
Para los casos sospechosos de fiebre Q se deberán realizar los siguientes exámenes para detección de Coxiella burnetii:
Las muestras para el estudio deben ser recolectadas de forma oportuna, tanto en pacientes de manejo ambulatorio como hospitalizados, rotuladas correctamente con todos los datos requeridos y considerando todas las indicaciones de bioseguridad y equipo de protección personal apropiado según corresponda para su envío a la sección de bacteriología del ISP.
Formulario B2 disponible en: https://formularios.ispch.cl/docPDF/EXT/formulario_b2.pdf y formulario B4 disponible en: https://formularios.ispch.cl/docPDF/EXT/formulario_b4.pdf
Otros estudios de laboratorio complementarios
A los casos sospechosos de fiebre Q se recomienda incluir en su estudio los siguientes exámenes
- Hemograma y VHS: suele tener recuento de leucocitos normales, discreta trombocitopenia en inicial, pudiendo evolucionar posteriormente con trombocitosis. VHS podría estar elevada.
- Perfil bioquímico , creatinina plasmática, proteína C reactiva (PCR), CPK total y procalcitonina (si está disponible), orina completa, electrolitos plasmáticos (ELP), gases arteriales o venosos, ácido láctico: alza de transaminasas hasta en el 85% de los casos e hiperbilirrubinemia en el 25%. PCR elevada, hiponatremia, y aumento de creatinquinasa (CK).
- Radiografía de tórax en dos proyecciones (PA y lateral): hasta en un 96% de los casos muestra condensación lobar o multilobar. En etapas muy precoces pudiese no evidenciarse infiltrados pulmonares. Es infrecuente el distress respiratorio.
- Tomografía axial computada de tórax si está disponible
- Hemocultivos periféricos (3 viales) 10 ml por punción (10:1) en paciente adulto
- Ecocardiografía Transtorácica (ETT): si se sospecha de Endocarditis Infecciosa Si ésta es negativa y la sospecha es alta, hacer Ecocardiografía Transesofágica.
Estudio de agentes respiratorios
- Panel molecular respiratorio en muestra de secreción obtenida por aspirado nasofaríngeo o hisopado nasofaríngeo.
- Cultivo cuantitativo de secreción respiratoria obtenida por aspirado traqueal (ATC) si el paciente está intubado (TOT)
- Cultivo cuantitativo de lavado bronquio-alveolar (LBA) si se realiza fibrobroncoscopía.
- Detección de MO respiratorios por panel molecular (Virus respiratorios Influenza A, Influenza B, Coronavirus).
- Los casos que cumplan con la definición de IRA Grave, derivar a Subdepto. Enfermedades Virales del ISP, según protocolo establecido con formulario de IRAG https://formularios.ispch.cl/docPDF/EXT/formulario_14_IRA_grave.pdf
Estudio de agentes gastrointestinales en pacientes con deposiciones líquidas
- Coprocultivo corriente y búsqueda dirigida de Campylobacter sp.
Referencias
1.- Fiebre Q (infección por Coxiella burnetii). En Red Book Informe 2015 del comité sobre enfermedades infecciosas.
2.- Eldin, C et al. From Q fever to Coxiella burnetii Infection: a paradigm Change. Clinical Microbiology reviews. Vol 30(1): 115-171;
3.- Ministerio de Salud de Chile. Protocolo de manejo clínico de los casos. Santiago, Minsal 2017.
Actualizado el 20 de noviembre de 2017.